Панел на F.D.A. гласува срещу лекарството за Алцхаймер на Biogen
- Здравеопазване
- Източник: Reuters
- Текст:
 Снимка: unsplash.com
Снимка: unsplash.com
В петък група от външни съветници към Американската администрация по храните и лекарствата гласува, че не е доказано, че потенциалното лечение на Алцхаймер от Biogen Inc забавя прогресирането на болестта. Това е остър укор към служителите на агенцията, които по-рано тази седмица похвалиха лекарството, пише Reuters.
F.D.A. все още може да реши да одобри лекарството адуканумаб, което го прави първото ново лечение на Алцхаймер от десетилетия. Но групата от научни съветници ясно изрази съмненията си относно лечението.
Няколко от 11-те членове на групата изразиха недоволство, че първоначалната гледна точка на F.D.A. за адуканумаб, която беше оповестена публично в сряда, беше предубедена към благоприятен резултат за Biogen. Тези коментари на персонала на F.D.A. допринесоха за увеличението на акциите на Biogen.
Агенцията даде „изключително много обяснения за противоречивите резултати", каза д-р Калеб Александър, професор по епидемиология и медицина в Johns Hopkins Bloomberg School of Public Health.
Панелът гласува с „не" на три въпроса, свързани с това дали едно-единствено успешно голямо проучване на адуканумаб е достатъчно доказателство за ефективността на лекарството, като се има предвид явният провал на второ голямо проучване. Те поставиха под съмнение позицията на F.D.A., че тестването на лекарството на ранен етап е достатъчно подкрепящо, за да компенсира неуспеха на второто основно проучване.
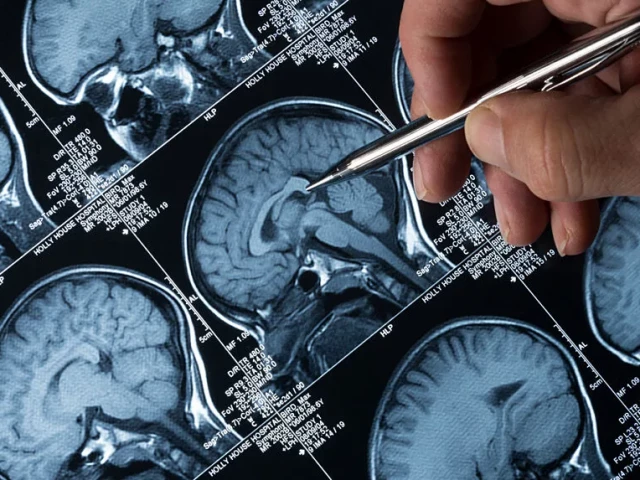
Петима членове на групата гласуваха с „да“ на въпроса дали адуканумаб има ефект върху нивата на амилоидна плака в мозъка на хората, диагностицирани с ранна болест на Алцхаймер, но шестима гласуваха „несигурно“ по въпроса.
Данните от изследванията включват много „червени флагове“, заяви членът на комисията д-р Аарон Кеселхайм, доцент в Harvard Medical School.
„Ще продължим да работим с F.D.A., тъй като тя завършва прегледа на нашето заявление", заяви Biogen в изявление.
Очаква се F.D.A. да вземе решение за лекарството до март и не е длъжна да следва препоръките на групата.
Болестта на Алцхаймер е шестата водеща причина за смърт в Съединените щати и има „дълбока и огромна неудовлетворена медицинска нужда" за нови лечения, каза Били Дън, директор по неврологични продукти към Центъра за оценка и изследване на лекарствата към F.D.A., по време на срещата.
В петък консултативният комитет изслуша и показания на редица хора, страдащи от болестта на Алцхаймер, включително няколко, които заявиха, че адуканумаб им се е отразил добре, докато са били част от тестването на лекарството.
„От първа ръка знаем, че това е помогнало на Кевин", каза Ким Бонъм, говорейки за съпруга си, който е бил диагностициран с болестта на Алцхаймер през 2016 г.
През октомври миналата година Biogen съживи плановете си да търси одобрение за адуканумаб месеци след като заяви, че независим анализ на безполезността на двете основни проучвания показва, че е малко вероятно да успеят.
Компанията заяви, че е променила посоката си, след като нов анализ показва, че висока доза от лекарството може да забави прогресията на заболяването.
По-рано тази седмица служителите на F.D.A. заявиха, че данните от едно от проучванията „предоставят основните доказателства за ефективност", както и клинично значим ефект от лечението.
Те казаха, че неуспехът на второ голямо проучване не накърнява констатациите от положителното проучване.
Още по темата във
facebookСподели тази статия в:

Борсовите цени на газа в Европа се променят слабо спрямо разчетната цена от понеделник

Петролът поевтинява с над 1% заради намаляване на опасенията от прекъсвания в доставките

Словакия отказа да възстанови доставките на електроенергия за Украйна

Гърция започва строителството на най-големия си обществен кооперативен соларен парк

САЩ забавят оръжейните доставки за Европа

Електронните магазини разчитат най-много на намаленията за увеличаване на продажбите си

Отровени бебешки храни откриха в Австрия

Как се хранят потомците на столетниците